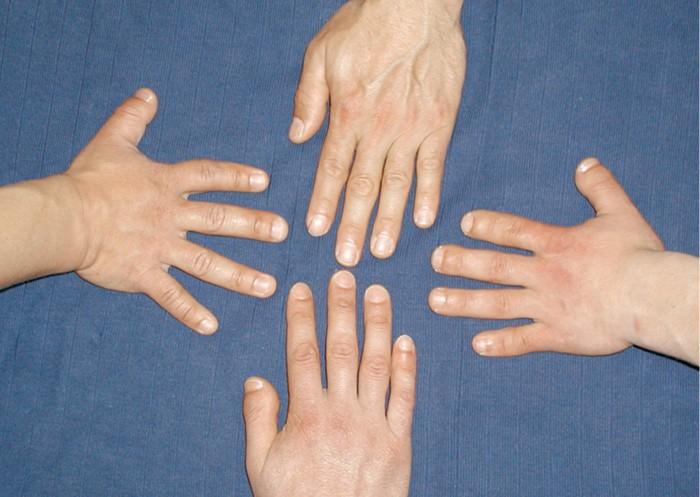
一個相關遺傳病家庭中的短指。圖像來源: Sylvia Bähring
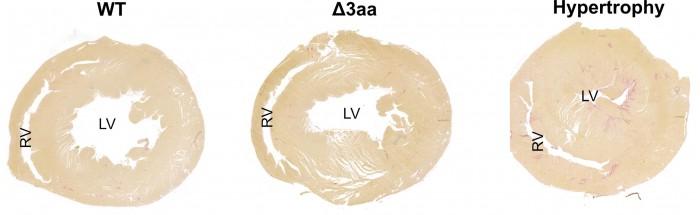
通過正常心髒(左)、通過其中一個突變體心髒(中間)和通過一個嚴重肥大的心髒(右)的橫截麵。在後者中,左心室被擴大了。圖像來源: Anastasiia Sholokh, MDC
(神秘的地球uux.cn)據cnBeta:柏林的科學家們幾十年來一直在研究一種奇怪的遺傳性疾病,這種疾病導致某些家庭中的一半人擁有令人震驚的短小手指和異常的高血壓。如果不加以治療,受影響的人往往在50歲時死於中風。柏林馬克斯-德爾布呂克中心(MDC)的研究人員在2015年發現了這種情況的起源,並在五年後利用動物模型進行了驗證:磷酸二酯酶3A基因(PDE3A)的突變導致其編碼的酶變得過度活躍,改變了骨骼生長並導致血管增生,造成高血壓。
其對高血壓相關的損害具有免疫力
馬克斯-德爾布呂克中心錨定信號實驗室負責人、德國心血管研究中心(DZHK)的科學家Enno Klußmann博士說:"高血壓幾乎總是導致心髒變得更弱,"Klußmann解釋說,由於它必須麵對更高的壓力進行泵送,該器官試圖加強其左心室。"但最終,這導致了心肌的增厚--被稱為心髒肥大--這可能導致心髒衰竭,大大降低其泵送能力"。
然而,這並不發生在短指和PDE3A基因突變的高血壓患者身上。Klußmann說:"由於現在部分但尚未完全了解的原因,他們的心髒似乎對通常由高血壓造成的損害有免疫力。"
這項研究是由馬克斯-德爾布呂克中心、柏林夏裏特大學和DZHK的科學家進行的,並已發表在《循環》雜誌上。除了Klußmann之外,最終作者還包括馬克斯-德爾布呂克中心的教授Norbert Hübner和Michael Bader,以及來自實驗和臨床研究中心(ECRC)的Sylvia Bähring博士,該中心是夏裏特和馬克斯-德爾布呂克中心的聯合機構。
該團隊包括來自柏林、波鴻、海德堡、卡塞爾、林堡、呂貝克、加拿大和新西蘭的其他43名研究人員,他們最近發表了關於該基因突變的保護作用的研究結果--以及為什麽這些發現可能改變未來治療心力衰竭的方式。該研究有四位第一作者,其中三位是馬克斯-德爾布呂克中心的研究人員,一位是ECRC的研究人員。
具有相同效果的兩種突變
科學家們對患有高血壓和手足徐動(HTNB)綜合症--即高血壓和異常短小的手指的人類患者以及大鼠模型和心肌細胞進行了測試。這些細胞是由被稱為誘導多能幹細胞的特殊工程幹細胞培育而成。在測試開始前,研究人員改變了細胞和動物中的PDE3A基因,以模擬HTNB突變。
Bähring報告說:"在我們檢查的病人中,我們遇到了一個以前未知的PDE3A基因突變。以前的研究總是顯示該酶的突變位於催化域之外--但我們現在發現了一個突變就在這個域的中心。令人驚訝的是,這兩個突變具有相同的效果,即它們使酶比平時更加活躍。這種過度活躍加快了細胞的重要信號分子之一,即cAMP(環狀腺苷單磷酸酯)的降解,它參與了心肌細胞的收縮。"Bähring懷疑:"有可能這種基因修改導致兩個或多個PDE3A分子聚集在一起,從而更有效地工作。"
蛋白質保持不變
研究人員使用了一個大鼠模型--由Max Delbrück中心的Michael Bader實驗室用CRISPR-Cas9技術創建--試圖更好地了解突變的影響。Klußmann說:"我們用藥劑異丙腎上腺素治療動物,這是一種所謂的β受體激動劑。這種藥物有時用於末期心力衰竭的病人。眾所周知,異丙腎上腺素會誘發心髒肥大。然而令人驚訝的是,這種情況發生在基因修飾的大鼠身上,其方式與我們在野生型動物身上觀察到的相似。與我們的預期相反,現有的高血壓並沒有加劇這種情況,他們的心髒很明顯地受到了異丙腎上腺素這種效應的保護。"
在進一步的實驗中,研究小組調查了心肌細胞的特定信號級聯中的蛋白質是否因突變而發生變化,如果是,則需要確定是哪些蛋白質。通過這一化學反應鏈,心髒對腎上腺素作出反應,並在興奮等情況下加速跳動。腎上腺素激活了細胞的β受體,使其產生更多的cAMP。PDE3A和其他PDEs通過化學方式改變cAMP來阻止這一過程。"Klußmann說:"然而,我們發現突變型和野生型大鼠在蛋白質和RNA水平上都沒有什麽區別。
細胞液中發現更多的鈣
PDE3A對cAMP的轉化並不隻是發生在心肌細胞的任何地方,而是在一個儲存鈣離子的管狀膜係統附近。這些離子釋放到細胞的細胞膜中,觸發了肌肉收縮,從而使心髒跳動。收縮後,鈣被一個蛋白質複合物泵回儲存。這個過程也是由PDE在局部調節的。
Klußmann和他的團隊假設,由於這些酶在鈣泵周圍的局部區域過度活躍,應該有較少的cAMP--這將抑製泵的活動。Klußmann實驗室的成員、該研究的四位第一作者之一Maria Ercu博士說:"在基因修飾的心肌細胞中,我們實際上表明,鈣離子在細胞膜中的停留時間比平時更長。這可能會增加細胞的收縮力。"
激活而不是抑製
Klußmann解釋說:"PDE3抑製劑目前被用於急性心力衰竭的治療,以增加cAMP水平。使用這些藥物的常規治療將迅速消耗心肌的力量。我們的發現表明,不是抑製PDE3,而是--相反--選擇性地激活PDE3A可能是預防和治療高血壓引起的心髒損傷(如肥厚性心肌病和心力衰竭)的一種新的和大大改進的方法。"
但他說,在這之前,需要對該突變的保護作用進行更多的說明。"我們已經觀察到PDE3A不僅變得更加活躍,而且它在心肌細胞中的濃度也降低了,"該研究人員的報告補充說前者有可能通過寡聚作用來解釋--一種涉及至少兩個酶分子一起工作的機製。"在這種情況下,我們也許可以開發出人工啟動局部寡聚的策略--從而模擬出對心髒的保護作用。
(责任编辑:娛樂)

